
Существует ряд международных требований (GMP, GDP, GSP) в которых сказано, что должна быть проведена валидация склада (фармацевтического, аптечного, дистрибьюторского). Этот процесс необходим для того, чтобы убедиться, что условия хранения лекарственных средств и материалов соответствуют указанной информации на упаковке, и учитывают температуру и относительную влажность воздуха.
Валидация склада - это процесс документального подтверждения того, что условия хранения продукции соблюдаются по всей площади и объему склада, на каждой полке, в местах хранения продукции.
Система вентиляции, кондиционирования и обогрева воздуха фармацевтического склада должна поддерживать заданные параметры температуры и, при необходимости, влажности воздуха независимо от времени суток, дня недели или климатического сезона. Соответственно, валидация аптечного склада должна охватывать эти условия и проводиться, как минимум, для двух наиболее критических климатических сезонов, когда температура окружающей среды выше или ниже, чем температура хранения продукции в складе, что соответствует работе систем охлаждения в «теплый» период года, и систем обогрева в «холодный» период года. При необходимости может также проводиться валидация транспорта.
Процесс проведения валидации склада
Первым этапом валидации склада может быть квалификация проекта. Она проводится до начала строительства и заключается в анализе проектной документации. Квалификация проекта не является обязательной, но именно на этой стадии могут быть выявлены критические ошибки, исправить которые после реализации проекта будет не просто, если вообще возможно.
 Квалификация монтажа проводится для новых складов или после их реконструкции. На этой стадии валидации фармацевтического склада в основном используются методы визуального контроля и сравнения со спецификацией. Проводится контроль наличия проектной документации, инструкций по эксплуатации и обслуживания элементов системы вентиляции, воздухоохладителей, нагревателей, систем автоматизации и диспетчеризации и др. Также необходимо проверить монтаж помещений, оборудования, трубопроводов и вспомогательных систем на соответствие действующим техническим чертежам и спецификациям.
Квалификация монтажа проводится для новых складов или после их реконструкции. На этой стадии валидации фармацевтического склада в основном используются методы визуального контроля и сравнения со спецификацией. Проводится контроль наличия проектной документации, инструкций по эксплуатации и обслуживания элементов системы вентиляции, воздухоохладителей, нагревателей, систем автоматизации и диспетчеризации и др. Также необходимо проверить монтаж помещений, оборудования, трубопроводов и вспомогательных систем на соответствие действующим техническим чертежам и спецификациям.
В соответствии с требованиями GDP на стадии квалификации монтажа необходимо определить требования к калибровке оборудования систем основного мониторинга и систем мониторинга температуры и проверить наличие сертификатов калибровки. Мы рекомендуем разделять процесс валидации аптечного склада и монтаж системы мониторинга, т. к. он должен проводиться после валидации склада и определения критических точек контроля. Не следует забывать, что система мониторинга также нуждается в валидации, а это уже совсем другой процесс.
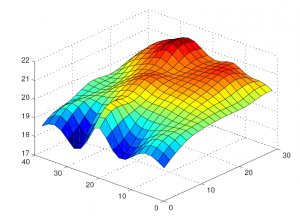
Квалификация функционирования проводится после успешного завершения квалификации монтажа. На этой стадии осуществляется картирование склада с использованием беспроводных даталоггеров температуры и влажности. Применение тепловизоров для этого процесса некорректно, ИК-термометры можно рассматривать лишь как дополнительный инструмент анализа рисков. По своей сути картирование склада (маппинг склада, температурная карта) — это определение наиболее холодной и горячей точки, а также точки в которой наблюдается максимальное колебание температуры. Эти измерения проводятся на протяжении минимум 24 часов с интервалом измерений 5-15 мин, количество даталоггеров определяется индивидуально для каждого помещения.
По результатам картирования склада должны быть определены критические точки контроля для пустого склада, в которые должны быть размещены датчики системы мониторинга.
После успешного завершения квалификации функционирования должны быть оформлены письменные методики (СРМ, СОП), должны быть завершены все работы не связанные с дистрибьюторской деятельностью, закончено проведение обучения операторов. Все это позволит эксплуатировать фармацевтический (аптечный) склад.
Квалификация эксплуатации проводится после успешного завершения стадий квалификации монтажа и функционирования. На этой стадии производится картирование склада, аналогично выполненному на стадии квалификации функционирования, только на складе загруженном продукцией. Измерения проводится на протяжении минимум 72 часов. Объем заполнения склада должен быть максимально возможным, для моделирования наихудшего случая с точки зрения препятствия распределения воздушным потокам, обычно это более 60%.
По результатам валидации аптечного склада должны быть определены критические точки контроля для склада с продукцией, в которые, если они отличаются от определенных на стадии квалификации функционирования, должны быть размещены дополнительные датчики системы мониторинга.
Стадию квалификации эксплуатации необходимо проводить минимум для «холодного» и «теплого» периодов года для подтверждения работы системы обогрева и охлаждения. В случае если система вентиляции, кондиционирования и отопления оснащена системой автоматического перехода тепло↔холод, необходимо проведение валидации 3 раза в год:
-
В холодный период — зимой, когда среднесуточная температура окружающей среды ниже температуры хранения;
-
В теплый период — летом, когда среднесуточная температура окружающей среды выше температуры хранения;
-
Переходной период — осень/зима или зима/весна, когда температура ночью опускается ниже температуры хранения, а днем — выше температуры хранения.
Повторная валидация склада
GDP говорит о том, что периодичность валидации необходимо основывать на анализе рисков, контроле изменений и обзорах данных системы мониторинга. Однако, как показывает практика анализ рисков проводится формально, с заведомо известным результатом, преследующим цель «ничего не изменено», система контроля изменений функционирует, в лучшем случае, по накопительной системе, об управлении изменениями речи не идет, а обзоры данных системы мониторинга проводятся без оценки тенденций, лишь по принципу «входит в пределы». Исходя из этого, в большинстве случаев, периодичность валидации 1 раз в 2, 3 или более лет является необоснованной, а при проведении валидации на таких складах выявляется большое количество проблем.
Лучшей практикой планирования и организации работ по валидации дистрибьютора лекарственных средств является установление периодичности ревалидации, которая охватывала бы теплый и холодный периоды года, на протяжении каждого года, для наработки достаточной статистики, которая и позволила бы снизить периодичность ревалидации.
Система мониторинга
Система мониторинга — это система, продуктом которой является текущая информация о техническом состоянии оборудования и его опасности с необходимыми комментариями (прогноз остаточного ресурса, предписания на неотложные действия персонала и т.д.) и заданным риском.
