
Існує ряд міжнародних вимог (GMP, GDP, GSP) в яких сказано, що повинна бути обов'язково проведена валідація складу (фармацевтичного, аптечного, дистриб'юторського). Цей процес необхідний для того, щоб переконатися, що умови зберігання лікарських засобів і матеріалів відповідають інформації, зазначеній на упаковці, а також враховують температуру і відносну вологість повітря.
Валідація складу - це процес документального підтвердження того, що умови зберігання продукції дотримуються по всій площі та об'єму складу, на кожній полиці в місцях зберігання продукції.
Система вентиляції, кондиціонування і обігріву повітря фармацевтичного складу повинна підтримувати задані параметри температури і, при необхідності, вологості повітря незалежно від часу доби, дня тижня або кліматичного сезону. Відповідно, валідація аптечного складу повинна охоплювати ці умови і проводитися, як мінімум, для двох найбільш критичних кліматичних сезонів, коли температура навколишнього середовища вище або нижче, ніж температура зберігання продукції в складі, що відповідає роботі систем охолодження в «теплий» період року, і систем обігріву в «холодний» період року. При необхідності може також проводитися валідація транспорту.
Процес проведення валідації складу
Першим етапом валідації складу може бути кваліфікація проекту. Вона проводиться до початку будівництва і полягає в аналізі проектної документації. Кваліфікація проекту не є обов'язковою, але саме на цій стадії можуть бути виявлені критичні помилки, виправити які після реалізації проекту буде не просто, або взагалі неможливо.
 Кваліфікація монтажу проводиться для нових складів або після їх реконструкції. На цій стадії валідації фармацевтичного складу в основному використовується методи візуального контролю і порівняння зі специфікацією. Проводиться контроль наявності проектної документації, інструкцій по експлуатації та обслуговування елементів системи вентиляції, повітряохолоджувачів, нагрівачів, систем автоматизації та диспетчеризації та ін. Також необхідно перевірити монтаж приміщень, обладнання, трубопроводів і допоміжних систем на відповідність діючим технічним кресленням і специфікаціям.
Кваліфікація монтажу проводиться для нових складів або після їх реконструкції. На цій стадії валідації фармацевтичного складу в основному використовується методи візуального контролю і порівняння зі специфікацією. Проводиться контроль наявності проектної документації, інструкцій по експлуатації та обслуговування елементів системи вентиляції, повітряохолоджувачів, нагрівачів, систем автоматизації та диспетчеризації та ін. Також необхідно перевірити монтаж приміщень, обладнання, трубопроводів і допоміжних систем на відповідність діючим технічним кресленням і специфікаціям.
Відповідно до вимог GDP на стадії кваліфікації монтажу необхідно визначити вимоги до калібрування обладнання систем основного моніторингу та систем моніторингу температури і перевірити наявність сертифікатів калібрування. Ми рекомендуємо розділяти процес валідації аптечного складу і монтаж системи моніторингу, так як він повинен проводитися після валідації складу і визначення критичних точок контролю. Не слід забувати, що система моніторингу також потребує валідації, а це вже зовсім інший процес.
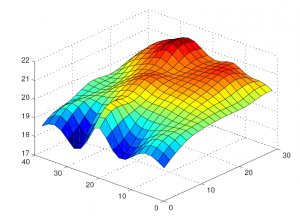
Кваліфікація функціонування проводиться після успішного завершення кваліфікації монтажу. На цій стадії здійснюється картування складу з використанням безпровідних даталогерів температури і вологості. Застосування тепловізорів для цього процесу некоректно, ІК-термометри можна розглядати лише як додатковий інструмент аналізу ризиків. За своєю суттю картування складу (маппінг складу, температурна карта) - це визначення найбільш холодної та гарячої точки, а також точки, в якій спостерігається максимальне коливання температури. Ці вимірювання проводяться протягом мінімум 24 годин з інтервалом вимірювань 5-15 хв, кількість даталоггерів визначається індивідуально для кожного приміщення зберігання.
За результатами картування складу повинні бути визначені критичні точки контролю для порожнього складу, в які повинні бути розміщені датчики системи моніторингу.
Після успішного завершення кваліфікації функціонування повинні бути оформлені письмові методики (СРМ, СОП), повинні бути завершені всі роботи не пов'язані з дистриб'юторською діяльністю, закінчено проведення навчання операторів. Все це дозволить використовувати фармацевтичний (аптечний) склад.
Кваліфікація експлуатації проводиться після успішного завершення стадій кваліфікації монтажу та функціонування. На цій стадії проводиться картування складу, аналогічно виконаному на стадії кваліфікації функціонування, тільки на складі завантаженому продукцією. Вимірювання проводиться протягом мінімум 72 годин. Обсяг заповнення складу повинен бути максимально можливим, для моделювання найгіршого випадку з точки зору перешкоди розподілу повітряним потоком, зазвичай це більше 60%.
За результатами валідації аптечного складу повинні бути визначені критичні точки контролю для складу з продукцією, в які, якщо вони відмінні від визначених на стадії кваліфікації функціонування, повинні бути розміщені додаткові датчики системи моніторингу.
Стадію кваліфікації експлуатації необхідно проводити мінімум двічі: для «холодного» і «теплого» періодів року для підтвердження роботи системи обігріву та охолодження. У разі якщо система вентиляції, кондиціювання та опалення оснащена системою автоматичного переходу тепло↔холод, необхідне проведення валідації 3 рази в рік:
-
У холодний період - взимку, коли середньодобова температура навколишнього середовища нижча за температуру зберігання;
-
У теплий період - влітку, коли середньодобова температура навколишнього середовища вища температури зберігання;
-
Перехідний період - осінь/зима або зима/весна, коли температура вночі опускається нижче температури зберігання, а вдень - вище температури зберігання.
Повторна валідація складу
GDP говорить про те, що періодичність валідації необхідно засновувати на аналізі ризиків, контроль змін та оглядах даних системи моніторингу. Однак, як показує практика, аналіз ризиків проводиться формально, із заздалегідь відомим результатом, переслідуючи мету «нічого не змінено», система контролю змін функціонує, в кращому випадку, за накопичувальною системою, про управління змінами мови не йде, а огляди даних системи моніторингу проводяться без оцінки тенденцій, лише за принципом «входить в межі». Виходячи з цього, в більшості випадків з періодичністю валідації 1 раз в 2, 3 або більше років є необґрунтованою, а при проведенні валідації на таких складах виявляється велика кількість проблем.
Кращою практикою планування і організації робіт по валідації дистриб'ютора лікарських засобів є встановлення періодичності ревалідації, яка охоплювала б теплий і холодний періоди року, протягом кожного року, для напрацювання достатньої статистики, яка і дозволила б знизити періодичність ревалідації.
Система моніторингу
Система моніторингу - це система, продуктом якої є поточна інформація про технічний стан устаткування та його небезпеки з необхідними коментарями (прогноз залишкового ресурсу, позпорядження на невідкладні дії персоналу тощо) і заданим ризиком.
